
Cell Reports Physical Science | 全息声镊引导下肝癌细胞球向肝胆类器官转移模型的构建
癌症转移是导致患者长期生存率下降的主要原因,构建一个能真实还原癌症转移过程的体外模型,是当前研究中的关键难题。传统的动物模型和二维细胞模型在模拟癌症转移上仍存在明显局限。近年来,三维细胞培养技术如类器官和细胞球,为体外建模带来了突破。然而,单一的类器官或者细胞球难以还原癌症转移过程中多组织间的动态互动。类组装体(Assembloid)是一种由多种细胞类型生成的具有空间结构的复杂类器官系统为模拟癌症转移提供了新路径。但现有构建方法,如3D打印和磁辅助组装,存在选择性差、毒性高等问题,难以精准还原转移过程。因此,发展一种安全稳定且高精度的新型技术,用于构建真实可靠的癌症转移模型,显得尤为迫切。
5月22日,中国科学院深圳先进技术研究院科学仪器所(筹)马腾研究员团队和哈尔滨医科大学田野教授团队合作在Cell旗下刊物 Cell Reports Physical Science上发表题为“Construction of a metastasis model for liver cancer spheroids to hepatobiliary organoids facilitated by holographic acoustic tweezers”的研究成果。该工作主要通过全息声镊科学仪器产生的具体生物医学应用,围绕全息声镊和三维细胞培养技术构建了类器官-细胞球在线组装平台,通过该平台构建了一种精准、可靠且具有多功能性的肝癌转移类组装体模型。此外,该研究还通过RNA测序技术评估了不同参数下声压对类器官和细胞球基因层面的影响,进一步的优化了操控参数。
在这项研究中,研究人员以主要聚焦于肝癌转移模型,并开发了一种组织工程技术—全息声镊(Holographic Acoustic Tweezers, HAT),通过个性化构建多重复合声场,实现了对肝癌细胞球的非接触式、精准操控。研究还利用人多功能干细胞(hiPSCs)诱导分化出可以同时表达肝脏和胆管结构功能的肝胆类器官(Hepatobiliary Organoids, HBOs),并利用表达绿色荧光蛋白(GFP)的人肝癌细胞系HuH-7构建肝癌细胞球。同时,通过免疫荧光染色和RNA测序分析,系统评估了不同参数下三维声场对肝胆类器官和细胞球安全性的影响,并进一步优化了操控参数。基于全息声镊和三维细胞培养技术,研究人员进一步开发了“类器官-细胞球在线组装平台”(Organoid-Spheroid Online Assembly Platform, OSOAP),用于构建体外单灶性及多灶性肝癌转移模型,并通过免疫荧光与Bulk RNA测序验证模型的可靠性。实验结果表明,该肝癌转移模型可以可视化肝癌浸润周围肝胆系统的过程,并且可以上调表达肝癌转移过程中特异性的信号通路。
为了展示该模型的多功能性和通用性,研究人员还在体外通过乙醇刺激构建了可以表达酒精性肝病相关病理生理过程的类器官。并通过该平台评估了酒精性肝病(Alcoholic Liver Disease, ALD)类器官与正常肝胆类器官对肝癌细胞球侵袭的易感性。免疫荧光染色的定量分析显示,肝癌细胞球对酒精性肝病类器官的浸润程度明显大于对正常肝胆类器官的浸润程度。
总结而言,该研究验证了三维声场对三维细胞培养模型的基因安全性影响,并开发了“类器官-细胞球在线组装平台”(OSOAP),成功构建了一个精准、可靠且具有多功能性的肝癌转移模型。本研究有望为癌症转移机制的研究提供一种全新的策略与平台。
中国科学院深圳先进技术研究院实习硕士生李嘉龙是该论文的第一作者。中国科学院深圳先进技术研究院马腾研究员和郑海荣研究员及哈尔滨医科大学田野教授为该论文的通讯作者。该研究获得医学成像科学与技术系统全国重点实验室、国家高性能医疗器械创新中心支持以及国家自然科学基金、国家重点研发计划、深圳市科技项目、工业和信息化部制造业高质量发展专项等基金资助。

文章上线截图
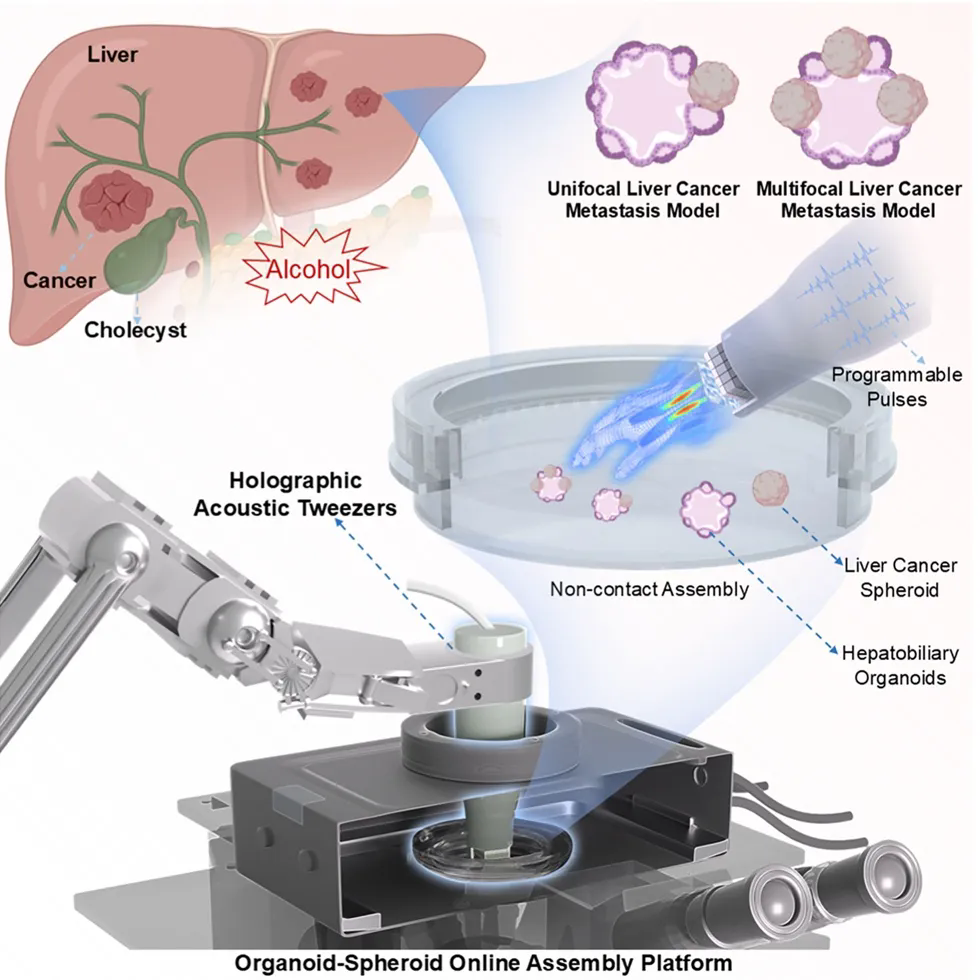
通过类器官-细胞球在线组装平台构建肝癌转移模型示意图
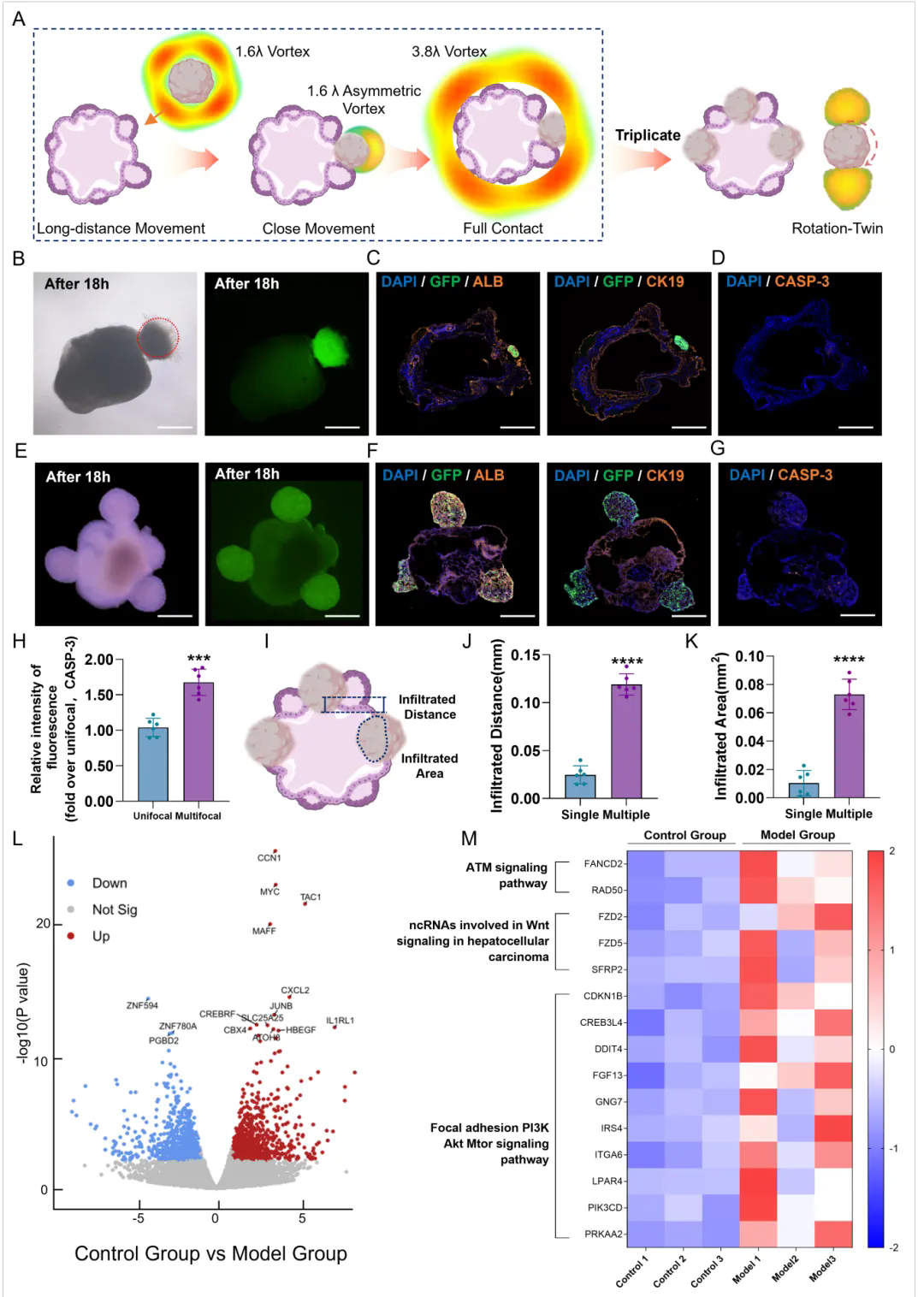
肝癌转移模型的构建以及细胞和基因层面验证的实验结果
附件下载: