
Advanced Science | 颅骨搬移术治疗创伤性脑损伤取得突破
创伤性脑损伤(Traumatic brain injury, TBI)是由头部受到突然的外部机械力,例如打击、撞击、震动或穿透而导致的脑损伤。我国每年TBI的人群发病率约为60/10万人,是导致死亡和残疾的主要原因。TBI目前主要的治疗方法包括急性期颅内压调控、神经保护药物干预、微创手术治疗以及术后康复。值得注意的是,大多TBI患者遗留持续性神经功能障碍,因此后遗症康复是TBI治疗策略的重要组成部分,目前尚缺乏有效的治疗方法可以减轻TBI的继发性脑损伤并改善长期预后。
颅骨搬移术(Cranial bone transport, CBT)是一种基于Ilizarov牵拉成组织技术理论上衍生的外固定技术,持续牵拉断裂骨组织的机械传导不仅能促进骨骼再生,还可诱导微小血管、神经等多种组织的再生。目前研究发现颅骨和脑膜之间存在微小的连接通道,颅骨骨髓中的免疫细胞可通过这些通道快速迁移至脑膜,参与炎症或损伤修复。本研究团队前期研究中已经证明CBT通过改善血管生成、神经生成和脑膜淋巴功能来促进缺血性卒中大鼠模型(大脑中动脉闭塞)的神经功能恢复,此外还发现CBT能够显著促进脑膜淋巴管的再生,并增强其引流功能,从而改善阿尔茨海默病转基因小鼠(5xFAD)的认知能力,减少脑内淀粉样蛋白沉积,并有效缓解神经炎症 。
近日,中国科学院深圳先进技术研究院生物医药与技术研究所李刚研究员联合香港中文大学医学院在CBT治疗TBI大鼠模型的研究方面取得了重要突破性进展,相关成果以"A novel cranial bone transport technique repairs skull defect and minimizes brain injury outcome in traumatic brain injury rats"为题,发表在国际权威期刊Advanced Science上。
该研究创新性地将CBT疗法应用于TBI大鼠模型,实现了神经再生与骨缺损修复的双重治疗突破。研究证实,CBT治疗不仅显著激活脑膜淋巴管功能,有效减轻神经炎症反应并降低磷酸化tau蛋白的病理性沉积,从而明显改善TBI大鼠的认知功能、空间记忆及运动协调能力,而且还同步促进颅骨缺损区域的新骨形成。
研究团队成功设计并制造CBT大鼠外固定支架,TBI大鼠模型建立24小时后,在颅骨缺损区域旁大通过截骨取骨瓣(直径 5 mm),经过3天潜伏期后,在骨缺损部位以0.25mm/12小时的速度进行缓慢的骨瓣搬运过程,持续10天后拆除外固定架。CBT操作过程简单且安全,治疗期间不会破坏硬脑膜和脑组织。研究结果发现,CBT治疗14天后脑皮质和海马中NeuN+神经元数量显著增加,TBI大鼠记忆增强,认知功能改善,运动能力恢复加快。利用Alexa Fluor 647标记的卵清蛋白对脑膜淋巴管功能进行评估后发现脑膜和颈深部淋巴结中的卵清蛋白量增加,损伤皮质中的磷酸化tau蛋白也在治疗后减少,说明CBT治疗后脑膜淋巴管引流功能也得到增强。此外,接受CBT治疗的TBI大鼠皮质和海马中Iba1标记的小胶质细胞减少,细胞活化形态减轻,提示CBT减轻了神经炎症。有趣的是,当研究团队将MAZ51(血管内皮生长因子受体3的抑制剂)注射进大鼠脑脊液内,从而减弱脑膜淋巴管引流功能后,CBT的治疗效果亦被消除,这一结果进一步验证了脑膜淋巴系统在CBT治疗中的核心作用。在治疗2个月后,CBT疗法仍表现出持续性的治疗效益,此外CBT加速了TBI大鼠颅骨缺损修复,骨缺损部位成骨标志物表达增加。研究团队和杭州求是医院合作,初步利用CBT对两例脑外伤患者进行了临床治疗,试验性治疗取得显著疗效,2名患者术后神经功能改善明显,实现骨缺损区域的有效再生。因此,基于现有证据,CBT疗法独特的神经保护和骨修复双重作用机制,使其成为TBI领域极具应用前景的创新性治疗策略,值得开展更深入的转化医学研究。
中国科学院深圳先进技术研究院生物医药与技术研究所运动系统再生医学技术研究中心主任李刚研究员为该论文的通讯作者,香港中文大学医学院白珊珊和陆轩博士为共同第一作者。该文章获得国家自然科学基金、国家重点研发计划、香港特别行政区研究资助局、香港健康医学研究基金、深圳市科技计划等科技项目支持。

论文上线截图
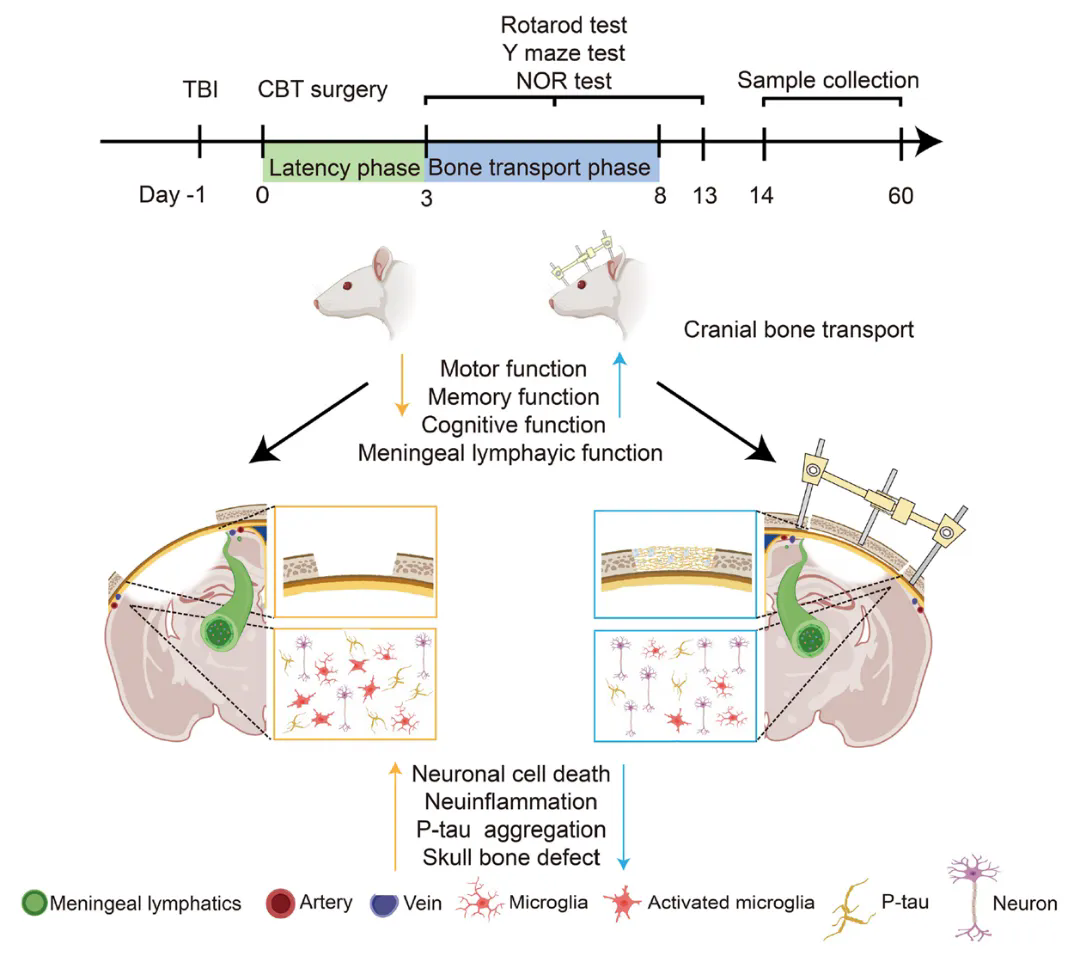
CBT治疗促进TBI大鼠神经功能恢复原理图
附件下载: